Heeft een scheet ook moleculen?!
Ja, een scheet bevat ook moleculen! Alles wat je ruikt of proeft, bestaat uit moleculen, en dat geldt ook voor de gassen die vrijkomen bij een scheet. Als je een wind wilt ‘bouwen’, heb je de volgende moleculen nodig: stikstof, waterstof, koolstofdioxide, zuurstof en methaan. Deze 5 moleculen zorgen voor 99% van je scheet en dit deel ruik je niet. Dit zijn dus de belangrijkste moleculen die in een scheet voorkomen:
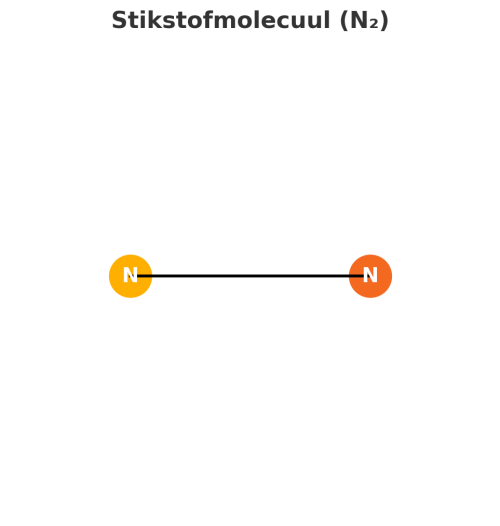
1. Stikstof (N₂)
Uitleg: Stikstof is het meest voorkomende gas in de lucht die we inademen, en het maakt ook het grootste deel van een scheet uit. Dit gas is geurloos.
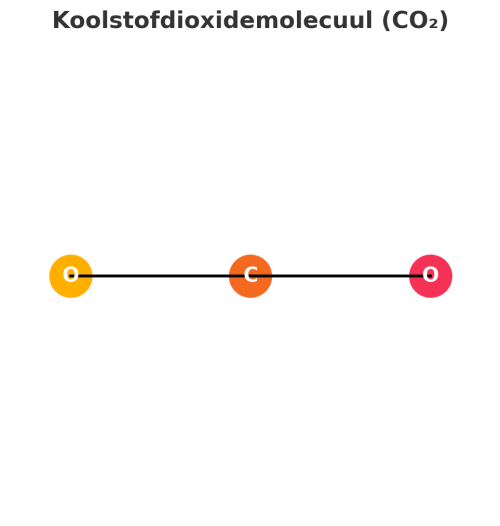
2. Koolstofdioxide (CO₂)
Uitleg: Dit gas ontstaat in je darmen door de werking van bacteriën die voedsel afbreken. Ook dit gas is geurloos.
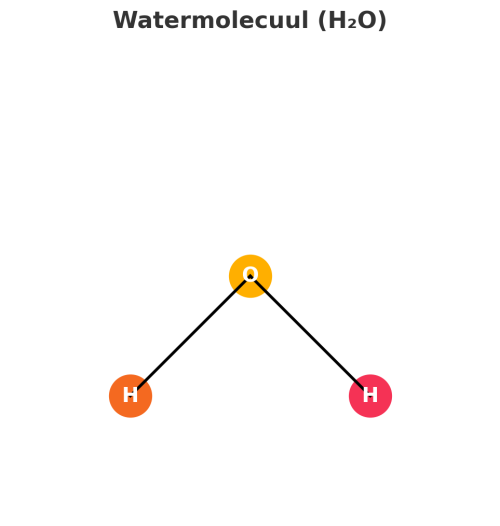
3. Waterstof (H₂)
Uitleg: Bacteriën in je darmen produceren waterstof tijdens de fermentatie van koolhydraten. Het is ook geurloos, maar kan soms ontvlambaar zijn.
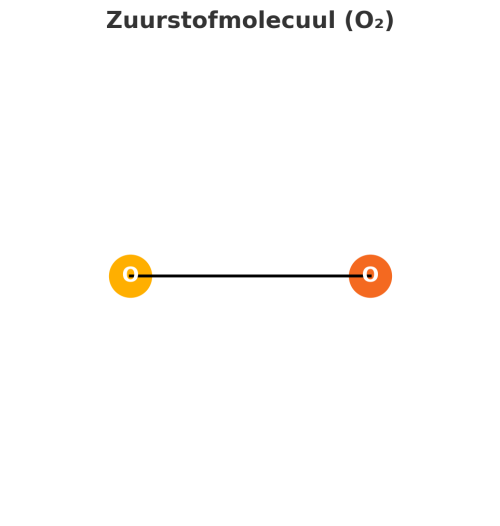
4. Zuurstof (O₂)
Uitleg: Zuurstof adem je de hele dag in en zo komt het dus in je lichaam. Dit is ook geurloos.
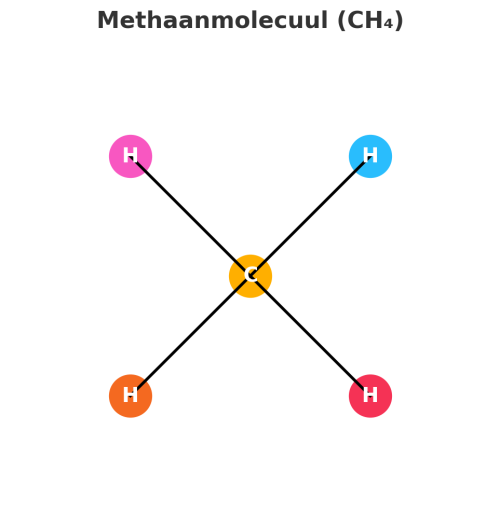
5. Methaan (CH₄)
Uitleg: Dit gas wordt geproduceerd door bepaalde soorten darmbacteriën. Niet iedereen produceert methaan, maar als het er is, draagt het bij aan de geurloosheid van een scheet.
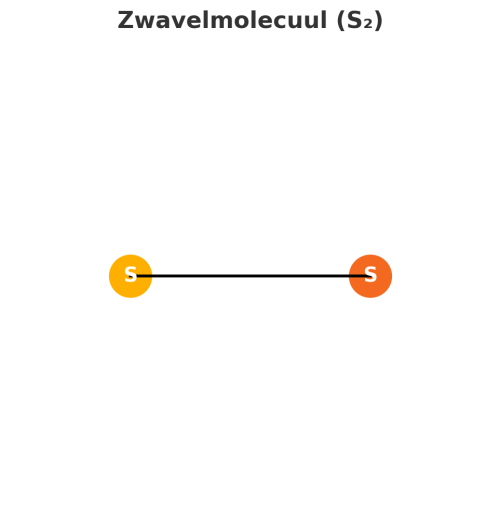
5. Zwavelverbindingen
Percentage: Minder dan 1%, maar verantwoordelijk voor de geur.
Voorbeelden van moleculen:Waterstofsulfide (H₂S): Dit molecuul ruikt naar rotte eieren.
Methanethiol (CH₄S) en Dimethylsulfide (C₂H₆S): Deze veroorzaken andere typische scheetgeuren.
Uitleg: Zwavelverbindingen worden geproduceerd als bacteriën eiwitten afbreken die zwavelhoudende aminozuren bevatten.